Skip to content
Overview
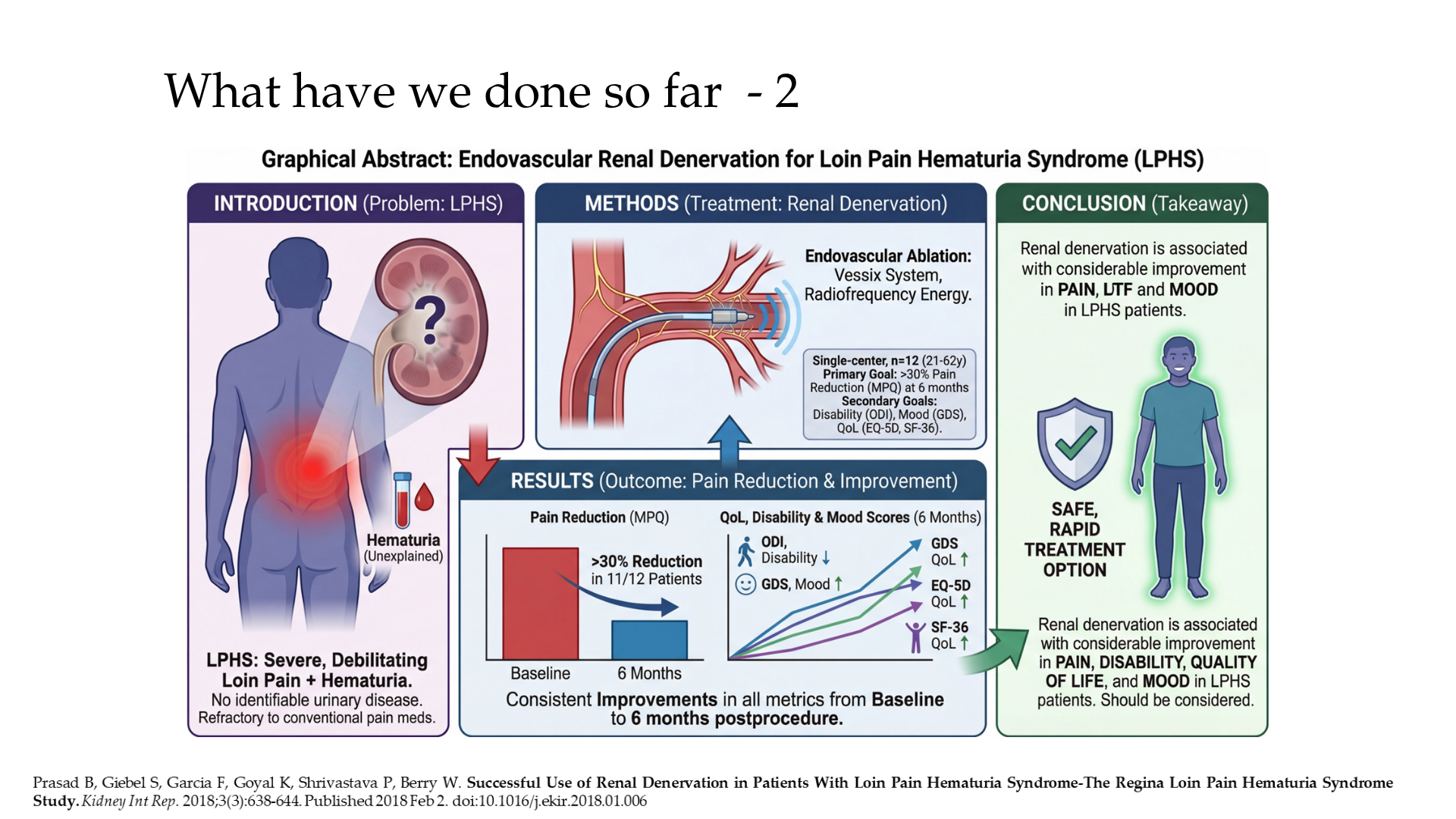
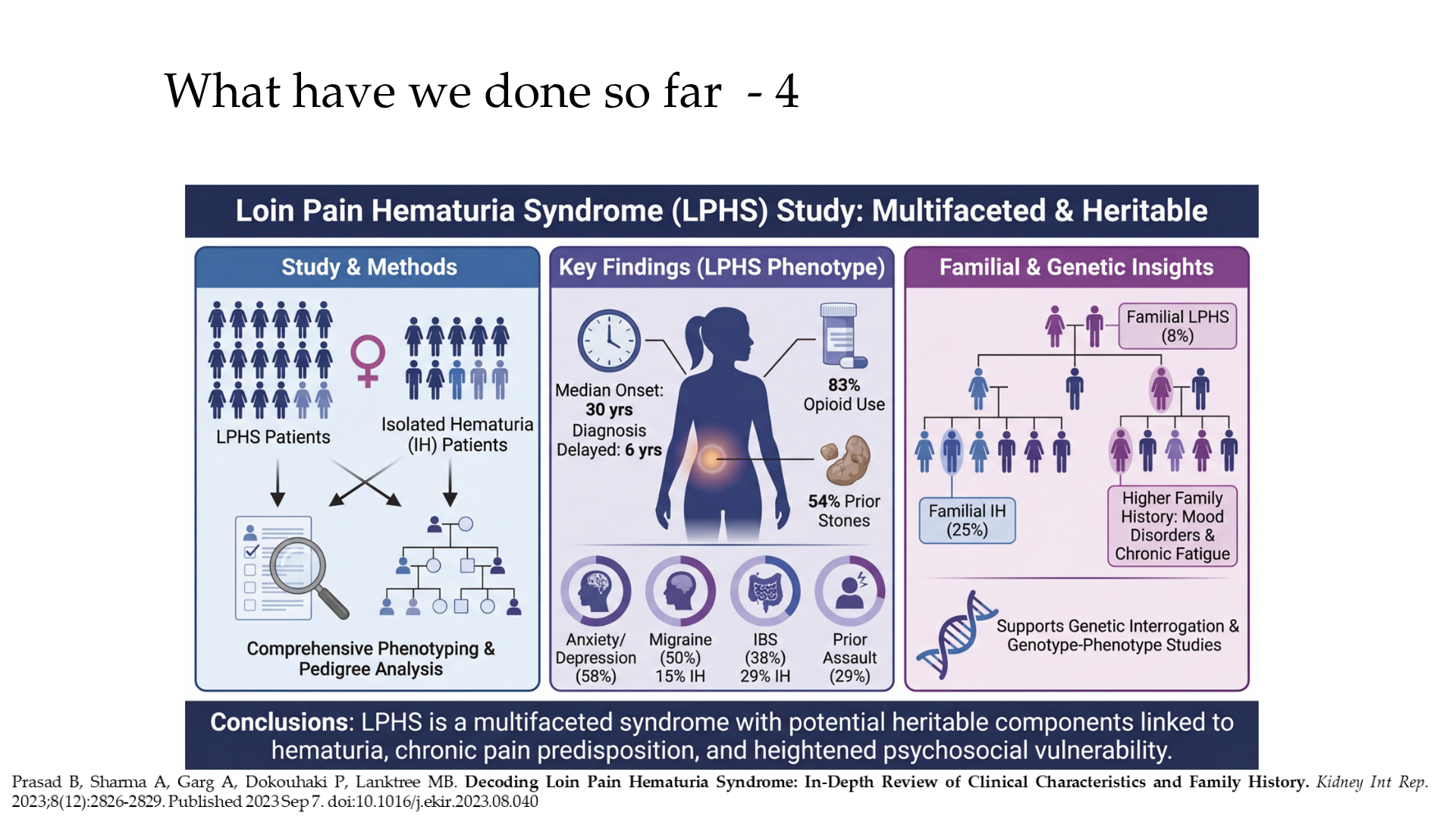
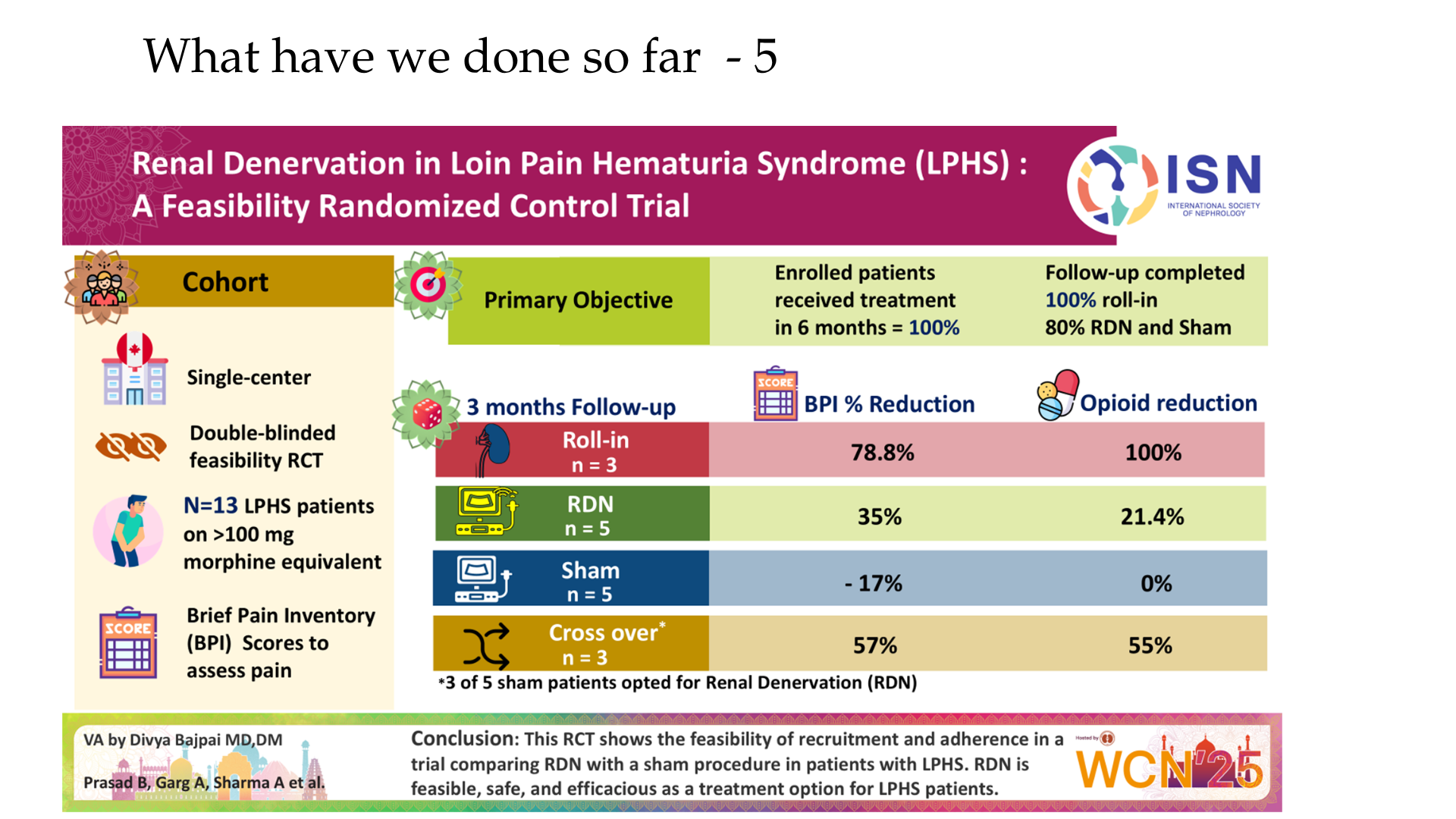
- Dr. Bhanu Prasad and team have advanced loin pain hematuria syndrome (LPHS) research through comprehensive phenotyping, multi-omics genotyping, and innovative pain therapies. Pioneered renal denervation (RDN) for refractory LPHS pain, demonstrating feasibility and symptom relief in case series/feasibility randomized controlled trial (RCT), reducing opioid needs without urological intervention
Genomics Insights:
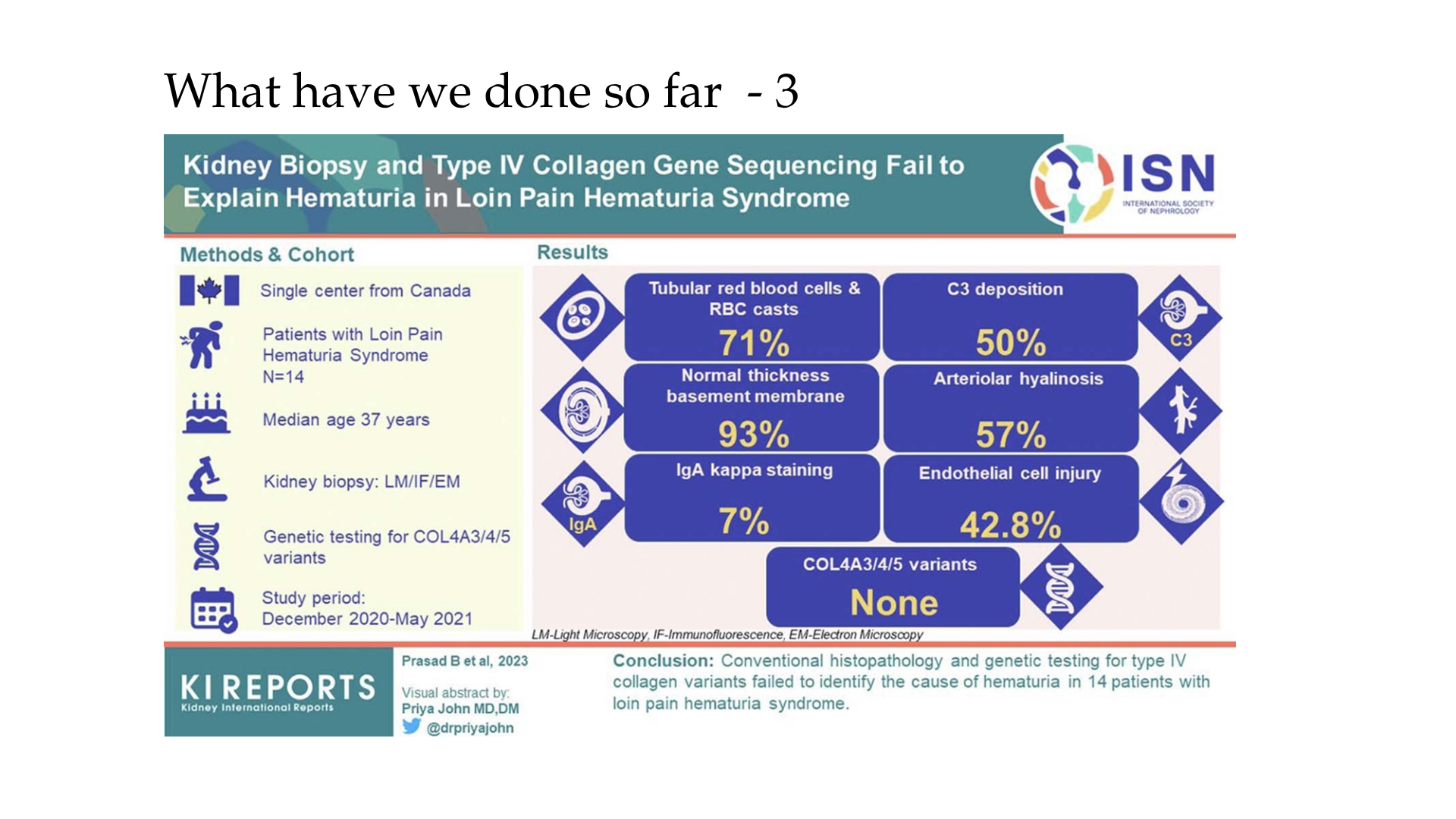
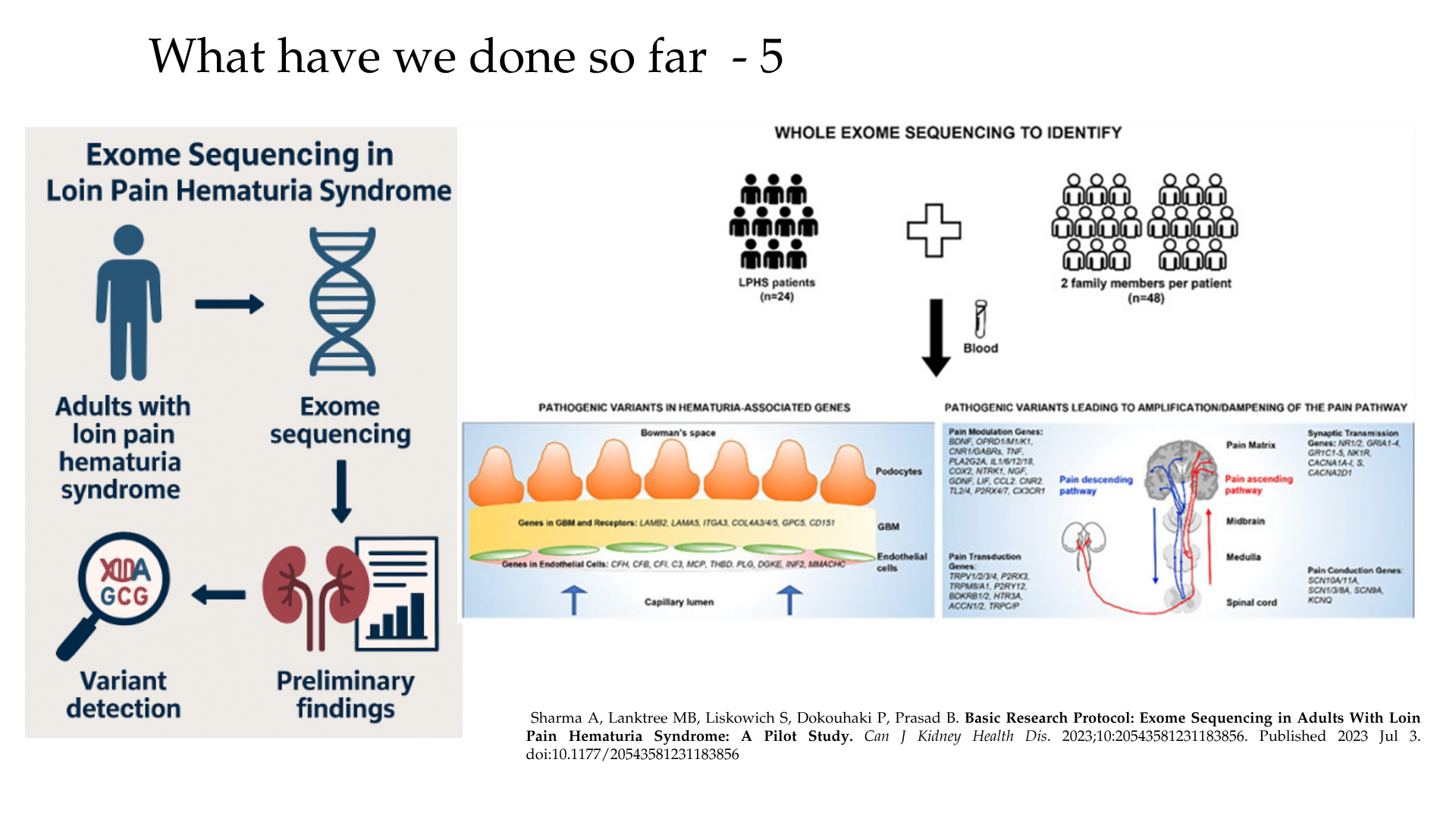
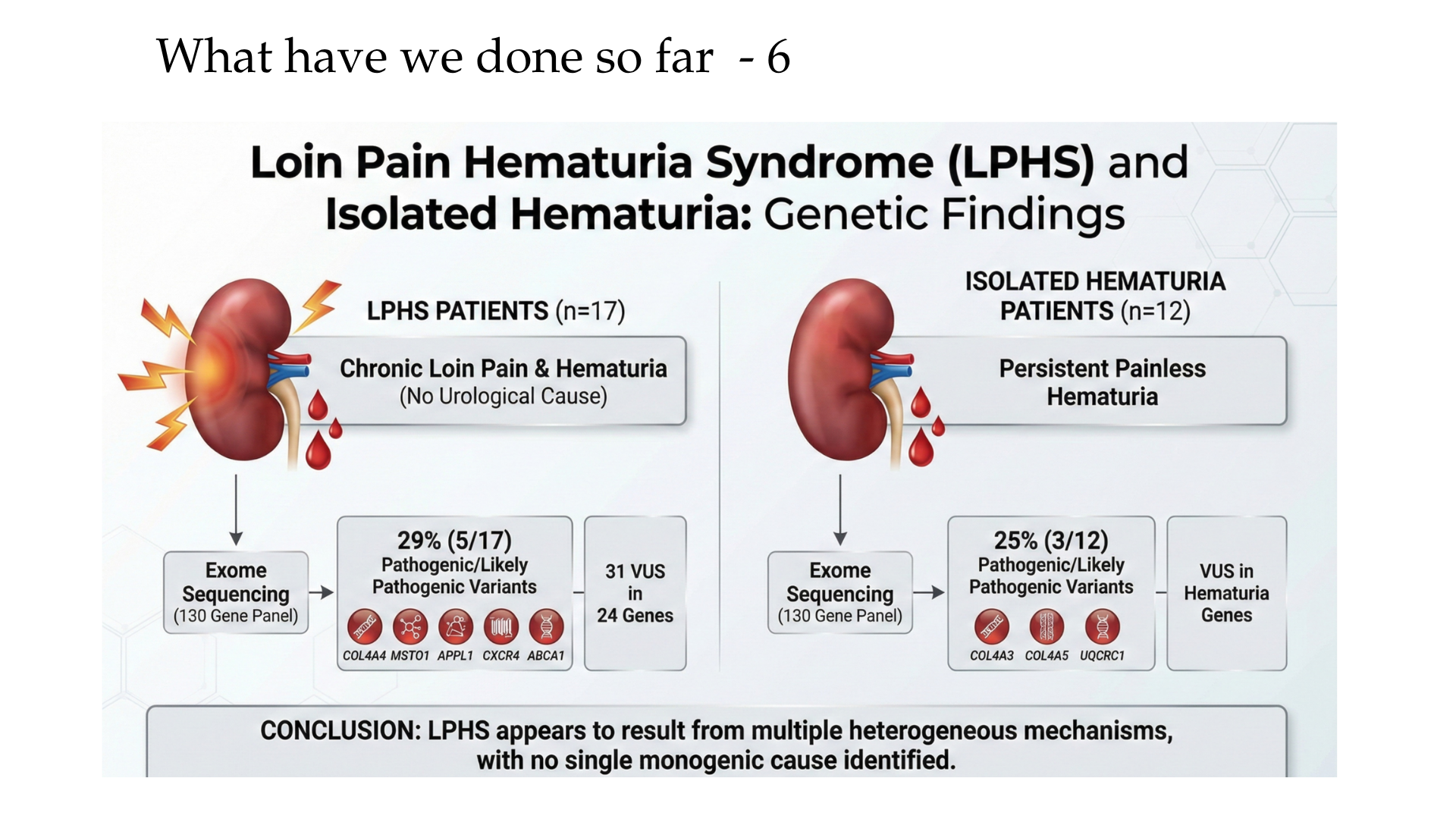
- Whole exome sequencing (WES) in LPHS adults identified candidate variants in glomerular endothelium, basement membrane, podocyte, and pain pathway genes (e.g., COl4A3-5, MSTO1, APPL1, CXCR4, and ABCA1), suggesting heterogeneous molecular drivers beyond classic mechanisms.
Therapeutic Advances:
- This integrated approach, WES/WGS/RNAseq to precision pain management, lays the groundwork for LPHS molecular therapies.
What is LPHS
- LPHS is a rare kidney-related condition, affecting about 1 in 8,000 people.
- It most commonly affects young women in their 20s and 30s.
- The main symptom is severe, persistent pain in the sides or lower back (loin pain).
- Patients also experience blood in the urine, which can be visible or only detectable under a microscope.
- Standard tests often show no kidney or urinary tract disease, making diagnosis challenging.
- Pain is chronic and often resistant to regular pain medications, including opioids.
- Patients often see many doctors and visit emergency departments frequently before diagnosis.
- LPHS significantly impacts quality of life, affecting daily activities and work.
- The exact cause of pain is not fully understood, but multiple triggers may contribute.
- Pain signals travel from the kidney to the spinal cord through specific nerve fibers, which can be targeted for treatment.